큰사진보기
|
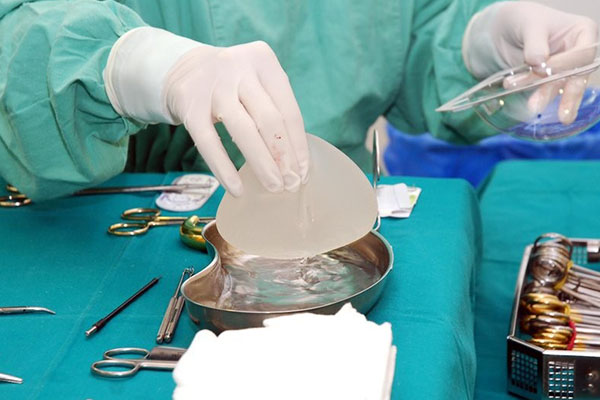
| ▲ 16일 식약처는 가슴 보형물 수술로 인한 BIA-ALCL 환자가 지난 13일 최초로 보고됐다고 밝혔다. |
| ⓒ 연합뉴스 | 관련사진보기 |
가슴 보형물을 가슴에 이식하는 수술을 받았다가 '희귀암' 판정을 받은 환자가 우리나라에서 처음으로 발견됐다.
해당 보형물은 보톡스 등 성형수술에 필요한 재료를 만드는 앨러간(Allergan)사가 만든 제품이다. 지난달 24일 미국 FDA(Food and Drug Administration)는 앨러간사가 만든 4개 '거친 표면 가슴 보형물'이 역형성 대세포 림프종(BIA-ALCL)이라 불리는 희귀암을 일으킬 가능성이 있다고 밝혔다. 그러면서 앨러간사에 이 제품의 '리콜'을 권했다.
16일 식품의약품안전처(아래 식약처)는 앨러간사의 거친 표면 가슴 보형물을 이식한 환자에게서 BIA-ALCL을 확인했다고 밝혔다. 이는 면역체계와 관련된 희귀암의 한 종류다. 가슴에 덩어리가 만져진다거나, 가슴이 부풀어 오르는 등의 증상을 일으킨다.
식약처에 따르면, 이번에 BIA-ALCL의 확진을 받은 환자는 40대 여성이다. 약 7~8년 전 가슴 보형물 이식 수술을 받았다가 최근 한쪽 가슴에 붓기가 생겨 지난 6일 성형외과를 찾은 것으로 알려졌다. BIA-ALCL이 의심된다는 성형외과 의견에 따라 대학병원으로 옮겨진 여성은 지난 13일 '희귀암이 맞다'는 최종 진단을 받았다.
이날 식약처는 수입업체 및 제조업체와 함께 부작용으로 인한 치료비 보상 등 대책을 수립하고 있고 있다고 밝혔다. 이어 유방 보형물 부작용 조사 등 환자 등록연구를 통해 안전관리에 나설 것이라고 덧붙였다.
하지만 '가슴 보형물의 안전'을 둘러싼 논란은 쉽게 가라앉지 않을 것으로 보인다. 지금까지 식약처는 대한성형외과학회의 의견을 바탕으로, BIA-ALCL은 희귀한 질병이고, 발견되면 완치 확률이 높다는 이유로 이식 수술을 받은 환자들에게 예방 차원의 보형물 제거는 권하지 않아왔다. 쉽게 말해 증상이 생기지도 않았는데 병이 생길 것을 걱정해 보형물을 뺄 필요는 없다는 것이다.
식약처 관계자는 14일 <오마이뉴스>와의 통화에서도 "우리나라에서 한 번도 발견된 적 없는 희귀한 암인 만큼 크게 우려할 필요가 없다"고 말했다. 그럼에도 불구하고 이날 BIA-ALCL의 환자가 우리나라에서 처음으로 나타난 것이다.
이날 한국 유방보형물 연구회 김재홍 위원장은 "정말 '희귀한 병'이 맞는지 식약처가 우리나라 이식 환자들 가운데 몇 명을 표본 조사할 필요가 있다"면서 "가슴 보형물로 인한 부작용을 막기 위해, 최소 1년에 한 번씩은 병원을 방문해 가슴 검진을 받아야 한다"고 말했다.